2024年8月19日,合肥星眸生物科技有限公司(以下简称“星眸生物”)宣布其自主研发的基因治疗I类创新药“XMVA09注射液”的第2项新药临床试验(IND)申请已获得国家药品监督管理局(NMPA)批准。今年3月,XMVA09注射液针对湿性年龄相关性黄斑变性(wAMD)适应症的IND申请获得CDE临床默示许可,此次新批准的适应症为糖尿病性黄斑水肿(DME)。作为星眸生物的战略合作伙伴,派真生物对此次成功获批表示热烈祝贺!我们期待与星眸生物继续携手,加速推进XMVA09注射液的临床应用和商业化进程,造福更多患者。
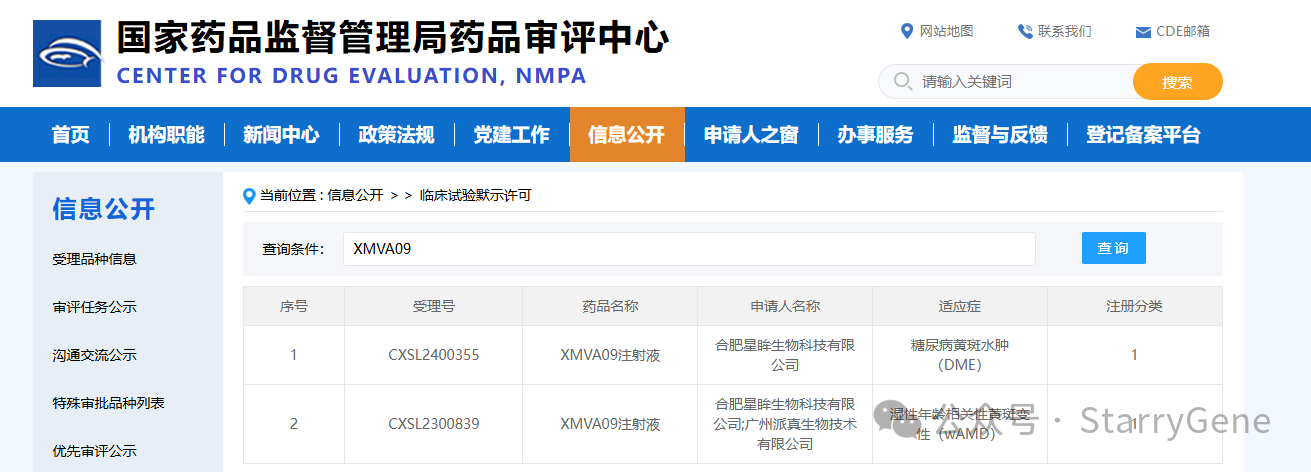
图片来源:CDE官网
糖尿病性黄斑水肿是糖尿病患者人群中一种常见的眼部并发症,主要影响视网膜中央的黄斑区域。黄斑是负责视觉清晰度的重要部位,当该区域发生水肿时,会导致视力下降甚至失明。治疗该眼部疾病的核心目标是维持并改善视力,临床治疗需求巨大。目前,抗血管内皮生长因子(anti-VEGF)是临床实践中最为安全、有效的治疗靶点。
XMVA09注射液是星眸生物自主研发的基因治疗药物,相比于传统抗体治疗药物1-3个月的注射周期,基因治疗药物可产生持续的治疗作用,有望实现一次注射便终身有效,极大地造福患者。XMVA09注射液采用全新的AAV衣壳,通过玻璃体腔内注射即可感染到紧贴脉络膜病灶的视网膜色素上皮层(RPE)细胞,为后续临床应用提供了更便捷的途径。此外,XMVA09注射液采用双抗设计,同时靶向血管内皮生长因子(VEGF)和血管生成素-2(ANG-2)双靶点,提高了药物的治疗效果,增加了对于VEGF不敏感患者的覆盖范围。
星眸生物创始人、CEO才源博士表示:“DME适应症的IND获批,是对XMVA09注射液研发潜力的有力证明。我们致力于通过创新科技,推动眼科疾病治疗的边界。这一成就标志着我们在实现这一愿景的道路上迈出了坚实的步伐。我们期待XMVA09注射液能够在临床实践中为患者带来更多的光明与希望!”
星眸生物首席医学官苗博龙博士表示:“XMVA09注射液在wAMD适应症的临床研究中已显示出良好的安全性和疗效,DME适应症的获批,进一步验证了我们药物的广泛适用性和治疗潜力。我们相信,DME新适应症的获批将进一步扩大我们服务患者的能力,为糖尿病性黄斑水肿患者提供更多的治疗选择。”
派真生物非常荣幸参与星眸生物XMVA09注射液项目,提供从质粒到AAV的全套CMC服务,助力推进XMVA09注射液针对湿性年龄相关性黄斑变性(wAMD)适应症IND的临床研究获批。我们对其在基因治疗领域的创新和成就表示敬意和祝贺,并期待双方继续深入合作,共同推进生物医药产业的创新发展,为人类健康事业贡献力量。
